Ca-antagonisten B-blokkers, TCAs intoxicaties
Uitgangsvraag
Specifieke adviezen bij intoxicaties met calciumantagonisten en bètablokkers en TCA’s
Aanbeveling
Calciumantagonistintoxicatie

Bètablokkerintoxicatie

Behandeling van intoxicatie met tricyclische antidepressiva
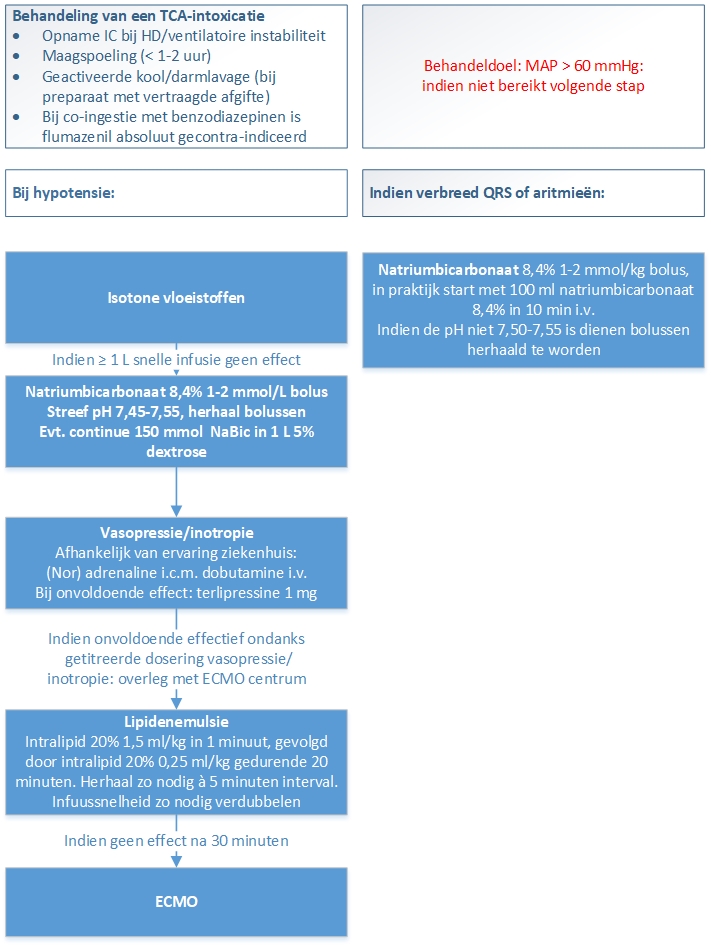
Onderbouwing
Achtergrond
Behandeling van calciumantagonist- en bètablokkerintoxicatie
De behandeling van een intoxicatie met bètablokkers en calciumantagonisten komt in grote lijnen overeen. Differentiatie tussen deze twee intoxicaties is in de klinische praktijk niet eenvoudig gezien het overeenkomstige klinisch beeld.
Op dit moment is de behandeling gebaseerd op expert opinions en ziet deze er als volgt uit: [Arbouw, 2013; Grouls, 2011]
|
Geneesmiddel |
Symptomen |
Diagnostiek |
Behandeling |
|
Bètablokker |
|
Vitale parameters ECG Glucose, elektrolyten, kreatinine, ureum Spiegelbepaling (incl. digoxine) |
Bij hypotensie:
|
|
Calcium antagonist: Fenylalkylamines (verapamil), dihydropyridines, diltiazem |
|
Vitale parameters ECG Glucose, elektrolyten, Nierfunctie, bloedgas Spiegelbepaling op indicatie(incl. digoxine) |
Bij hypotensie:
|
Samenvatting literatuur
Calciumantagonistintoxicatie
- Calciumantagonistintoxicatie kan leiden tot hypotensie, bradycardie en aritmieën; in ernstigere gevallen ontstaat cardiogene shock. [Grouls, 2011]
- Maagspoelen (< 1 uur) en geactiveerde kool kan overwogen worden bij patiënten die zich < 1-2 uur na intoxicatie melden. Darmlavage en geactiveerde kool zijn aangewezen in geval van intoxicatie met preparaten met vertraagde afgifte. [Grouls, 2011]
- Bij hypotensie/shock zijn er verschillende therapeutische opties beschikbaar:
Toedienen van isotone vloeistoffen is eerste keus bij hypotensie. [Graudins, 2016] Gezien doorgaans euvolemische patiënt: volume ≥ 1 L (max 2 L gezien het risico op overvulling). [Grouls, 2011]
Glucagon
In case reports zijn de resultaten tegenvallend en glucagon heeft daarom geen plaats in de behandeling van een calciumantagonistintoxicatie. [Grouls, 2011; Graudins, 2016; St-Onge, 2014]
Calcium
Intoxicatie met een calciumantagonist leidt tot intracellulaire hypocalciëmie. Toediening van calcium i.v. kan de cardiale geleiding verbeteren, heeft een positief inotroop effect en kan leiden tot bloeddrukstijging. . [Newton, 2002]
In ernstige intoxicaties die zich presenteren met hypotensie is calcium monotherapie onvoldoende effectief.. [Graudins, 2016; St-Onge, 2014]
Insuline/glucose
Ten tijde van shock prefereren myocyten koolhydraten boven vrije vetzuren als energiebron. Insulinetherapie verhoogt het intracellulaire transport van glucose in de myocyt. Verder leidt insuline tot toename van de plasmaconcentratie van calcium wat een positief inotroop effect heeft. [Graudins, 2016]
Een systematische review naar gebruik van insuline/glucosetherapie bij calciumantagonistintoxicatie laat het volgende zien: [St-Onge, 2014]
|
Interventie |
Uitkomst |
Bijwerkingen |
Opmerkingen |
|
Glucose/ |
HD verbetering in 1 van 2 observationele studies |
Hypoglycemie Hypokaliëmie |
5 case reports positieve uitkomst |
Dosering van insuline/glucosetherapie is niet goed onderzocht.
Bij de behandeling wordt een bolus van 1 U/kg aangehouden, om vervolgens een onderhoudsdosering van 0,5 U/kg/u te starten welke na 30 minuten opgetitreerd kan worden.
Catecholamines
Van geen enkele catecholamine is er bewijs voor consistente effectiviteit bij een calciumantagonistintoxicatie. [Graudins, 2016; St-Onge, 2014]
Een systematische review vermeldt het volgende: [Newton, 2002]
|
Interventie |
Uitkomst |
Bijwerkingen |
Opmerkingen |
|
Fenylephrine |
Geen effect |
|
|
|
Vasopressine |
3 patiënten toename RR indien toegevoegd aan andere vasopressor |
|
|
|
Adrenaline |
|
Hyperglycemie Toename lactaat |
|
|
Dopamine |
|
Tegenstrijdige resultaten |
|
|
Noradrenaline |
|
Idem |
|
|
Atropine |
|
|
|
|
Isoprenaline |
Verbetering RR en PR in 4 patiënten |
|
|
|
Levosimendan |
|
|
Positief inotroop, toename respons myocyt op calcium en contractiliteit |
Gebaseerd op ervaring wordt bij een calciumantagonistintoxicatie het volgende aangehouden: [Graudins, 2016]
Adrenaline à eerste keus
Vasopressine, Isoprenaline à tweede keus
Atropine bij ernstige bradycardie
Amrinone, levosimendan à derde keus
Lipidenemulsie
Lipidenemulsie zou positieve effecten op de hemodynamiek kunnen hebben door het versnellen van de klaring/distributie van lipofiele geneesmiddelen.[Fettiplace, 2015] Dit effect is het grootst bij lipofiele medicatie. [Graudins, 2016; Grouls, 2016; St-Onge, 2014; Sebe, 2015]
|
Geneesmiddel |
Vd (L/kg) |
|
Amlodipine |
12-21 |
|
Diltiazem |
1,9-4,4 |
|
Nifedipine |
0,8-1,6 |
|
Verapamil |
4-8,6 |
Na falen van insuline/glucosetherapie (refractaire hypotensie) is lipidenemulsie effectief gebleken bij intoxicaties met diltiazem, amlodipine en verapamil. [Sebe, 2015]
ECMO (extra corporele membraan oxygenatie)
Indien cardiogene shock niet reageert op bovenstaande middelen, kan ECMO toegepast worden. Enkele case reports laten positieve resultaten zien al dan niet in combinatie met Total Plasma Exchange. [Kolcz, 2007; Masson, 2012]
ECMO in het kader van een hartstilstand ten gevolge van intoxicatie leidt tot significant betere uitkomsten dan conservatieve behandeling. Deze significantie verdwijnt in het geval van cardiogene shock. [Masson, 2012]
ECMO is niet in ieder ziekenhuis beschikbaar. Verwijzing naar een centrum met ECMO zou vroegtijdig overwogen moeten worden.
Bètablokkerintoxicatie
- Bètablokkerintoxicatie kan leiden tot hypotensie en bradycardie; in ernstigere gevallen ontstaat cardiogene shock. [Arbouw, 2013]
- Darmlavage in combinatie met geactiveerde kool kan overwogen worden bij patiënten die zich < 2 uur na intoxicatie melden. Bij een kortere tijd tot melden na intoxicatie, kan overwogen worden hier voorafgaand maaglavage toe te passen. Volledige darmlavage en actieve kool zijn ook nadien aangewezen in geval van intoxicatie met preparaten met vertraagde afgifte. [Arbouw, 2013]Bij hypotensie/shock zijn er verschillende therapeutische opties beschikbaar:
Toedienen van isotone vloeistoffen is eerste keus bij hypotensie. [Arbouw, 2013]
Glucagon
- Glucagon heeft positieve inotrope en chronotrope effecten door stimulatie van adenylcyclase. [Harvey, 2011]
- Monotherapie met glucagon heeft geen effect in verschillende case series [Harvey, 2011]
Onderhoudsdosering glucagon is beperkt beschikbaar in de acute setting.
Calcium
Intoxicatie met een bètablokker leidt tot intracellulaire hypocalciëmie. Toediening van calcium i.v. kan de cardiale geleiding verbeteren, heeft een positief inotroop effect en kan leiden tot bloeddrukstijging. [Newton, 2002]
In ernstige intoxicaties die zich presenteren met hypotensie is calcium monotherapie onvoldoende effectief. [Newton, 2002]
Insuline/glucose
Ten tijde van shock prefereren myocyten koolhydraten boven vrije vetzuren als energiebron. Bètablokkers zorgen voor een verlaagde glucose-uptake ten gevolge van toegenomen insulineresistentie en hypo-insulinemie. Insulinetherapie is daarom een logische keus in geval van bètablokkerintoxicatie. Verder leidt insuline tot toename van de plasmaconcentratie calcium wat een positief inotroop effect heeft. [Harvey, 2011]
Dosering van insuline/glucosetherapie is niet goed onderzocht.
In de behandeling wordt een bolus van 1 U/kg aangehouden, om vervolgens een onderhoudsdosering van 0,5 U/kg/u te starten welke na 30 minuten opgetitreerd kan worden onder strikte, frequente glucose- en K-monitoring.
Catecholamines
Op basis van de eigenschappen van de verschillende bètablokkers zouden catecholamines effectief kunnen zijn. Gezien de verschillende receptorselectiviteit kan de respons afhankelijk van het type bètablokker verschillen. [Newton, 2002]
Tabel. Farmacologische eigenschappen van bètablokkers [Newton, 2002]
|
Betablokker |
Receptor |
Proteïne-binding |
T1/2 (uren) |
Biobeschikbaarheid (%) |
Distributievolume (l/kg) |
Vetoplosbaarheid |
Primair metabolisme |
Membraan stabilisatie |
|
Acebutolol |
Beta1 |
25 |
3-4 |
70 |
1,2 |
Laag |
Hepatisch |
+ |
|
Atenolol |
Beta1 |
5-10 |
6-9 |
50-60 |
1 |
Laag |
Renaal |
- |
|
Betaxolol |
Beta1 |
50 |
14-22 |
90 |
5-13 |
Laag |
Hepatisch |
+ |
|
Bisoprolol |
Beta1 |
30 |
9-12 |
80 |
3 |
Laag |
Renaal |
- |
|
Carteolol |
Beta1, Beta2 |
30 |
6 |
85 |
|
Laag |
Renaal |
+ |
|
Carvedilol |
Alfa1, Beta1, Beta2 |
25-35 |
6-8 |
20 |
1-2 |
Hoog |
Hepatisch |
+ |
|
Esmolol |
Beta1 |
55 |
9 min |
Niet |
2 |
Laag |
Erythrocyt esterase |
- |
|
Labetalol |
Alfa1, Beta1, Beta2 |
50 |
6-8 |
90 |
9 |
Matig |
Renaal |
- |
|
Metoprolol |
Beta1 |
10 |
3-4 |
90 |
4 |
Matig |
Hepatisch |
- |
|
Nadolol |
Beta1, Beta2 |
25-30 |
20-24 |
30 |
2 |
Laag |
Renaal |
- |
|
Penbutanol |
Beta1, Beta2 |
80-98 |
5 |
100 |
0,5 |
Hoog |
Hepatisch |
- |
|
Pindolol |
Beta1, Beta2 |
50 |
3-4 |
95 |
2 |
Matig |
Hepatisch |
+ |
|
Propranolol |
Beta1, Beta2 |
90 |
3-5 |
90 |
4 |
Hoog |
Hepatisch |
+ |
|
Sotalol |
Beta1, Beta2 |
0 |
7-15 |
80 |
2 |
Laag |
Renaal |
- |
|
Timolol |
Beta1, Beta2 |
10 |
4 |
90 |
2 |
Matig |
Hepatisch |
- |
Van geen enkele catecholamine is er bewijs voor consistente effectiviteit: [Newton, 2002]
- Dobutamine blijkt vaak niet effectief.
- Dopamine laat in enkele case studies een positief effect zien.
- Isoproterenol zou als bèta-adrenerge agonist theoretisch effectief kunnen zijn, maar behoeft ook hoge doseringen wat leidt tot dysritmie en vasodilatatie.
- Stimulatie van alfareceptoren verhoogt de kans op hartfalen.
- Fosfodiësteraseremmers (amrinone, milrinone) hebben positieve effecten laten zien. Echter, gezien het vasodilatatoire effect moet gelijktijdig gestart worden met een vasopressor. Ook is de T1/2 lang en wordt titratie daardoor bemoeilijkt.
Lipidenemulsie
Lipidenemulsie zou positieve effecten op de hemodynamiek kunnen hebben door het laten ontstaan van zogenaamde ‘lipid sink’. Dit effect is het grootst bij lipofiele medicatie. Deze eigenschappen staan in bovenstaande tabel vermeld.
- Na falen van insuline/glucosetherapie is lipidenemulsie effectief gebleken bij intoxicaties met carvedilol, propranolol en penbutanol. [Harvey, 2011; Cao, 2015]
- Verschillende case reports tonen aan dan lipidenemulsie niet effectief is bij intoxicaties met metoprolol. [Sebe, 2015; Cao, 2015]
ECMO
Indien cardiogene shock niet reageert op bovenstaande middelen, kan ECMO toegepast worden. Enkele case reports laten positieve resultaten zien al dan niet in combinatie met Total Plasma Exchange. [Kolcz, 2007; Masson, 2012]
- ECMO in het kader van een hartstilstand ten gevolge van intoxicatie leidt tot significant betere uitkomsten dan conservatieve behandeling. Deze significantie verdwijnt in het geval van cardiogene shock. [Masson, 2012]
- ECMO is niet in ieder ziekenhuis beschikbaar. Verwijzing naar een centrum met ECMO zou vroegtijdig overwogen moeten worden.
Behandeling van intoxicatie met tricyclische antidepressiva
Intoxicaties met tricyclische antidepressiva uiten zich in centrale effecten gekenmerkt door verwardheid, slaperigheid en in ernstige insulten en coma; anticholinerge effecten en cardiovasculaire effecten leiden tot tachycardie, hypertensie en in een later stadium bradycardie, aritmieën, hypotensie en in ernstige gevallen cardiogene shock. [Jansman, 2015]
Adviezen ten aanzien van de huidige behandeling, zien er zo uit: [Jansman, 2015]
|
Geneesmiddel |
Symptomen |
Diagnostiek |
Behandeling |
|
TCA |
|
Vitale parameters ECG Glucose, elektrolyten, nierfunctie Spiegelbepaling |
Bij hypotensie/shock:
|
TCA-intoxicatie
- Door trage absorptie, groot verdelingsvolume en enterohepatische recirculatie van zowel de primaire stof als metabolieten, resulteert TCA-inname in lange klinisch effecten; zeker bij overdosering. [Woolf, 2007]
- Morbiditeit en mortaliteit t.g.v. TCA-intoxicatie is voornamelijk het gevolg van aritmieën en hypotensie, die meer refractair wordt naar mate de acidose toeneemt. [Callaham, 1985]
Maagspoelen, geactiveerde kool
- TCA’s worden geabsorbeerd door geactiveerde kool. [Woolf, 2007]
- Er zijn geen goede studies uitgevoerd naar het effect van geactiveerde kool op de uitkomst van intoxicaties met TCA’s. [Woolf, 2007] Er is bewijs dat supportive care geen verschil in TCA-spiegel laat zien in vergelijking met behandeling met geactiveerde kool. [Woolf, 2007] Ook is er geen verschil in TCA-spiegel in patiënten die behandeld werden met maagspoeling versus maagspoeling én geactiveerde kool. [Woolf, 2007]
- Geactiveerde kool is het meest effectief < 1 uur na ingestie, maar laat bij gezonde vrijwilligers ook nog absorptievermindering zien van nortriptyline < 4 uur na ingestie. [Dawling, 1978]
- Absorptievermindering van amitriptyline d.m.v. geactiveerde kool is het meest effectief < 4 uur na ingestie, maar herhaalde giften gestart > 6 uur na ingestie laten nog steeds effect op absorptie zien. [Karkkainen, 1986]
- TCA’s hebben anticholinerge eigenschappen die zeker bij overdosering leiden tot vertraagde maagontlediging en verminderde intestinale peristaltiek. [Woolf, 2007]
- TCA-intoxicatie kan in sporadische gevallen leiden tot ileus, toxisch megacolon of darmischemie. In deze gevallen is orale toediening van medicatie (dus ook geactiveerde kool) gecontra-indiceerd. [Woolf, 2007]
- Natriumpolystereensulfaat heeft in vitro een beter effect dan geactiveerde kool op de Cmax van verschillende TCA’s : amitriptyline, clomipramine en doxepine. [Jamshidzadeh, 2014]
- Op basis van bovenstaande argumenten is maagspoeling aan te bevelen < 1-2 uur na ingestie.
- Geactiveerde kool is bij gezonde vrijwilligers effectief gebleken en goede studies in patiëntenpopulatie ontbreken. Op basis van mechanistische en farmacokinetische gronden is er een plaats voor gebruik van geactiveerde kool.
Darmlavage
- In het geval van een matig ernstige voorspelde intoxicatie met TCA door tabletten met gereguleerde afgifte, kan totale darmlavage overwogen worden. [O’Connor, 2006; NVIC, 2016]
Natriumbicarbonaat
- Verschillende reviews en case reports laten positieve effecten zien van bicarbonaat in het kader van TCA-intoxicatie. [Woolf, 2007]
- Het onderliggende werkingsmechanisme is niet geheel duidelijk, maar omvat de volgende onderdelen: [Vrijlandt, 2001]
> Door extra natrium wordt het remmende effect van TCA’s op cardiale natriumkanalen geantagoneerd;
> Door alkaliseren wordt de eiwitbinding van TCA in het bloed verhoogd;
> Door alkaliseren wordt de extracellulaire kaliumconcentratie verlaagd;
> Door het volume-effect van natriumbicarbonaat wordt hypotensie bestreden;
> Door natriumbicarbonaat wordt het remmende effect van TCA op calcium als second messenger geantagoneerd.
- Over de dosering van natriumbicarbonaat bij een TCA-intoxicatie bestaat geen hard wetenschappelijk bewijs. De meeste richtlijnen adviseren het geven van bolussen natriumbicarbonaat 1 mmol/ml (8,4%) 1-2 mmol/kg, met streef pH 7,45-7,55 en daarnaast een onderhoudsdosering van 150 mmol in 1 L 5% glucose om deze pH te behouden. [Bruccoleri, 2016]
- Aan de hand van een case report wordt gesuggereerd te streven naar pH 7,50-7,55 bij TCA-intoxcatie. Andere indicatoren zijn het geven van bolus natriumbicarbonaat bij QRS-complex > 111 ms of rechterasdeviatie > 120 graden. [Pierog, 2009]
Magnesiumsulfaat
- Er zijn verschillende case reports beschikbaar waarin magnesiumsulfaat (2 g bolus, vervolgens 3-20 mg/min i.v.) ventriculaire aritmieën laat verdwijnen. Het gesuggereerde werkingsmechanisme zou op basis van toegenomen intracellulair kalium zijn, daar magnesium een cofactor van membraan Na/K-ATP-ase is. [Citak, 2002; Emamhadi, 2012]
- Een RCT toont een significante verlaging van mortaliteit en verkorting van ligduur op de IC aan bij het gebruik van magnesiumsulfaat naast natriumbicarbonaat bij TCA-intoxicatie bij patiënten met pH < 7,2 en QRS-verbreding. [Emamhadi, 2012]
- Op basis van deze onderzoeken en de geringe bijwerkingen is er een plaats voor magnesiumsulfaat in de behandeling van TCA-intoxicatie. Met name patiënten met verbreed QRS of ventriculaire aritmieën kunnen baat hebben bij additionele magnesiumbehandeling.
Lipidenemulsie
- Er zijn verschillende case reports beschikbaar die een positief effect van lipidenemulsie op cardiale of neurologische toxiciteit laten zien bij TCA-intoxicatie, gegeven na conventionele therapie. [Cave, 2014; Cave, 2011; Levine, 2016]
- In een recent onderzoek wordt op basis van case reports gezien dat lipidenemulsie na therapie voor intoxicatie met lokale anesthetica, het vaakst positieve effecten bij amitriptyline-intoxicatie laat zien. [Muller, 2015]
- Bijwerkingen/nadelen van lipidenemulsie bestaan vooral uit moeilijkheden in laboratoriumbepalingen, hypertriglyceridemie en zelden pancreatitis. [Cao, 2015]
- Op basis van deze literatuur lijkt er een plaats voor het gebruik van lipidenemulsie bij de behandeling van TCA-intoxicatie, als therapie met natriumbicarbonaat en magnesium onvoldoende effectief is gebleken. In het geval van hemodynamische instabiliteit kan gelijktijdig gestart worden met inotropie/vasopressie.
Inotropie/vasopressie
- TCA’s grijpen op verschillende receptoren. Refractaire hypotensie is meestal het gevolg van alfa-1-receptor antagonisme. [Zuidema, 2007]
- Hoge doseringen catecholamines kunnen nodig zijn bij behandeling van hemodynamische instabiliteit t.g.v. TCA-intoxicatie. [Zuidema, 2007] Echter, deze doseringen brengen een hoog risico op bijwerkingen, met name aritmieën, met zich mee. [Zuidema, 2007]
- Een case report laat een positief effect zien op refractaire hypotensie van terlipressine (1 mg). Verder zijn er verschillende studies die laten zien dat vasopressine synergisitsch met catecholamines kan werken bij patiënten met cardiovasculair falen op de IC. [Zuidema, 2007]
- Op basis van bovenstaande kan het gebruik van inotropie en vasopressie nodig zijn in TCA-intoxicaties die zich presenteren met hemodynamische instabiliteit. Er is geen duidelijke evidence voor specifieke middelen.
- In het geval van refractaire hypotensie op standaard vasopressie en inotropie kan terlipressine een uitkomst bieden.
ECMO
- Indien cardiogene shock niet reageert op bovenstaande middelen, kan ECMO toegepast worden. Enkele case reports laten positieve resultaten zien al dan niet in combinatie met Total Plasma Exchange. [Kolcz, 2007; Masson, 2012]
- ECMO in het kader van een hartstilstand ten gevolge van intoxicatie leidt tot significant betere uitkomsten dan conservatieve behandeling. Deze significantie verdwijnt in het geval van cardiogene shock. [Masson, 2012]
- ECMO is niet in ieder ziekenhuis beschikbaar. Verwijzing naar een centrum met ECMO zou vroegtijdig overwogen moeten worden.
Referenties
- Arbouw MEL, Jansman FGA, Kieft H. Monografie bètablokkers. www.toxicologie.org; versie 4; aug 2013.
- Bruccoleri RE, Burns MM. A literature review of the use of sodium bicarbonate for the treatment of QRS widening. J Med Toxicol 2016; 12: 121-9.
- Callaham M, Kassel D. Epidemiology of fatal tricyclic antidepressant ingestion: implications for management. Ann Emerg Med 1985; 14: 1-9.
- Cao D, Heard K, Foran M, Koyfman A. Intravenous lipide emulsion in the emergency department: a systematic review of recent literature. J Em Med 2015; 48: 387-97.
- Cave G, Harvey M, Graudins A. Review article: intravenous lipid emulsion as antidote: a summary of published human experience. Em Med Australas 2011; 23: 123-141.
- Cave G, Harvey M, Willers J, Uncles D, Meek T, Picard J, Weinberg G. LIPAEMIC report: results of clinical use of intravenous lipide emulsion in drug toxicity reported to an online lipid registry. J med Toxicol. 2014; 10:133-142.
- Çitak A, Soysal DD, Ucsel R, Karabocuoglu M, Uzel N. Efiicacy of long duration resuscitation and magnesium sulphate in treatment in amitriptyline poisoning. Eur J Em Med 2002; 9: 63-6.
- Dawling S, Crome P, Braithwaite R. Effect of delayed administration of activated charcoal on nortriptyline absorption. Eur J Clin Pharmacol 1978; 14: 445-7.
- Emamhadi M, Mostafazadeh B, Hassanijirdehi M. Tricyclic antidepressant poisoning treated by magnesium sulfate: a randomized, clinical trial. Drug Chem Toxicol 2012; 35: 300-3.
- Fettiplace MR, Lis K, Ripper R, Kowal K, Pichurko A, Vitello D, et al. Multi-modal contributions to detoxification of acute pharmacotoxicity by a triglyceride micro-emulsion. J Control Release 2015; 198: 62-70.
- Graudins A, Lee HM, Druda D. Calcium channel antagonist and beta-blocker overdose: antidotes and adjunct therapies. Br J Clin Pharmacol 2016; 81: 453-61.
- Grouls RJE, Bindels AJGH, Roos AN. Monografie calciumantagonisten. www.toxicologie.org; Versie 4, juni 2011.
- Harvey M, Cave G, Lahner D, Desmet J, Prince G, Hopgood G. Insulin versus lipid emulsion in a rabbit model of severe propranolol toxicity: a pilot study. Crit Care Res Pract 2011; 361739.
- Jamshidzadeh A, Vahedi F, Farshad O, Seradj H, Najibi A, Dehghanzadeh G. Amitriptyline, clomipramine, and docepin adsorption onto sodium polystyrene sulfonate. Daru 2014; 22: 21.
- Jansman FGA, Kieft H. Monografie tricyclische antidepressiva. www.toxicologie.org; versie 3. 2015.
- Karkkainen, S, Neuvonen PJ. Pharmacokinetics of amitriptyline influenced by oral charcoal and urine pH. Int J Clin Pharmacol 1986; 24: 326-32.
- Kolcz J, Pietrzyk J, Januszewska K, Procelewska M, Mroczek T, Malec E. Extracorporeal life support in severe propranolol and verapamil intoxication. J Intensive Care Med 2007; 22: 381-5.
- Levine M, Hofman RS, Lavergne V, Stork CM, Graudins A, Chuang R, et al. Systematic review of the effect of intravenous lipid emulsion therapy for non-local anesthetics toxicity. Clin Toxicol 2016; 54: 194-221.
- Masson R, Colas V, Parienti JJ, Lehoux P, Massetti M, Charbonneau P, et al. A comparison of survival with and without extracorporeal life support treatment for severe poisoning due to drug intoxication. Resuscitation 2012; 83; 1413-7.
- Muller SH, Diaz JH, Kaye AD. Clinical applications of intravenous lipid emulsion therapy. J Anesth 2015; 29: 920-6.
- Newton CR, Delgado JH, Gomez HF. Calcium and beta receptor antagonist overdose: a review and update of pharmacological principles and management. Semin Respi Crit Care Med 2002; 23: 19-25.
- NVIC. Monografie amitriptyline. www.vergiftingen.info Geraadpleegd 2-2-2016
- OConnor N, Green S, Dargan P, Wyncoll D, Jones A. Prolonged clinical effects in modified-release amitriptyline poisoning. Clin Toxico (Phila) 2006; 44: 77-80.
- Pierog JE, Kane KE, Kane BG, Donovan JW, Helmick T. Tricyclic antidepressant toxicity treated with massive sodium bicarbonate. Am J Em Med 2009; 27: 1168e3-7.
- Sebe A, Disel NR, Acikalin Akpinar A, Karakoc E. Role of intravenous lipid emulsions in the management of calcium channel blocker and B-blocker overdose: 3 years experience of a university hospital. Postgrad Med 2015; 127: 119-24.
- St-Onge M, Dubé PA, Gosselin S, Guimont C, Godwin J, Archambault PM, et al. Treatment for calcium channel blocker poisoning: a systematic review. Clin Toxicol (Phila) 2014; 52: 926-44.
- Vrijlandt PJWS, Bosch TM, Zijlstra, JH, Tulleken JE, Ligtenberg JJM, Werf TS van der. Natriumbicarbonaatinfusie bij intoxicatie met tricyclische antidepressiva: aanbevolen ondanks gebrek aan wetenschappelijk bewijs. Ned Tijdschr Geneeskd 2001; 145: 1686-9.
- Woolf AD, Erdman AR, Nelson LS, Caravati EM, Cobaugh DJ, Booze LL, et al. Tricyclic antidepressant poisoning: an evidence-based consensus guideline for out-of-hospital management. Clin Toxicol (Phila) 2007; 45: 203-33.
- Zuidema X, Jager CP de. Terlipressin and tricyclic antidepressant intoxication. Neth J Med 2007; 65: 313-4.
- Zuidema X, Dunser MW, Wenzel V, Rozendaal FW, Jager CP de. Terlipressin as an adjunct vasopressor in refractory hypotension after tricyclic antidepressant intoxication. Resuscitation 2007; 72: 319-23.
Verantwoording
Autorisatiedatum en geldigheid
Laatst beoordeeld : 18-12-2017
Laatst geautoriseerd : 18-12-2017
Geplande herbeoordeling :
Jaarlijks wordt door de commissie richtlijnen van de Nederlandse Internisten Vereniging bepaald of actualisatie van de richtlijn nodig is. Indien actualisatie gewenst is, spant de Nederlandse Internisten Vereniging zich om de hiervoor noodzakelijke voorwaarden (bijvoorbeeld financiering, samenstelling werkgroep) te realiseren. Nieuwe of nog niet behandelde knelpunten kunnen aanleiding zijn tot actualisatie van de richtlijn.
Algemene gegevens
De richtlijnontwikkeling werd gefinancierd uit de Stichting Kwaliteitsgelden Medisch Specialisten (SKMS) en ondersteund door het bureau van de Nederlandse Internisten Vereniging en PROVA.
Doel en doelgroep
Doel
Het doel van deze richtlijn is de kwaliteit van zorg en patiëntveiligheid van patiënten met een acute intoxicatie te waarborgen en waar mogelijk te verbeteren. In deze richtlijn worden aanbevelingen geformuleerd die professionals in de zorg hiertoe de handvaten geven.
Doelgroep
De doelgroep van deze richtlijn zijn professionals die zich bezig houden met de opvang van patiënten, na een acute intoxicatie, in het ziekenhuis. Hieronder worden in ieder geval verstaan: spoedeisende hulp artsen, internisten (inclusief subspecialisaties zoals internisten acute geneeskunde en intensivisten op de intensive care), anesthesiologen, cardiologen, psychiaters en ziekenhuisapothekers. Maar, ook anderen kunnen deze richtlijn gebruiken.
Samenstelling werkgroep
Voor de ontwikkeling van deze richtlijn is een werkgroep geformeerd, onder voorzitterschap van dr. Kees Kramers, internist-klinisch farmacoloog. In de werkgroep hadden gemandateerde vertegenwoordigers van de belangrijkste beroepsverenigingen die te maken hebben met de opvang van patiënten met een acute intoxicatie zitting. Ook was een vertegenwoordiger van het Nationaal Vergiftigingen Informatie Centrum lid van de werkgroep. Om het patiëntenperspectief in de werkgroep te waarborgen, is de werkgroep aangevuld met een beleidsadviseur werkzaam bij Patiëntenfederatie Nederland. Tijdens de commentaarronde is een vertegenwoordiger van de Nederlandse Vereniging voor Anesthesiologie aan de werkgroep toegevoegd en is commentaar van de Nederlandse Vereniging voor Anesthesiologie toegevoegd. De werkgroep werd procedureel en methodologisch ondersteund door PROVA en logistiek door het bureau van de Nederlandse Internisten Vereniging. De ontwikkeling van deze richtlijn is gefinancierd vanuit een projectbudget door de Stichting Kwaliteitsgelden Medisch Specialisten.
- Dhr. dr. C. Kramers, internist - klinisch farmacoloog, Radboud Universitair Medisch Centrum, Nijmegen, namens de Nederlandse Internisten Vereniging, voorzitter
- Mw. drs. M.K. Tuut, epidemioloog, PROVA, Varsseveld, secretaris
- Dhr dr. H.J. van Leeuwen, Internist-intensivist, Ziekenhuis Rijnstate, Arnhem, namens de Nederlandse Vereniging voor Intensive Care
- Dhr. drs. D. Dekker, internist acute geneeskunde – klinisch farmacoloog, Universitair Medisch Centrum, Utrecht, namens de DAM, beroepsvereniging van internisten acute geneeskunde
- Mw. drs. G.D. van Dijken, SEH-arts KNMG, St. Antonius Ziekenhuis, Nieuwegein, namens de Nederlandse Vereniging voor Spoedeisende Hulp Artsen
- Dhr. drs. J. Benedictus, Patiëntenfederatie Nederland, Utrecht, namens Patiëntenfederatie Nederland
- Dhr. dr. D. W. de Lange, intensivist - toxicoloog, Universitair Medisch Centrum Utrecht, namens het Nationaal Vergiftigingen Informatie Centrum (NVIC) van het UMC Utrecht
- Dhr. drs. S.J.C. ten Napel, SEH-arts KNMG, Ziekenhuis Rijnstate, Arnhem, namens de Nederlande Vereniging van Spoedeisende Hulp Artsen
- Dhr. dr. R.E.J.H. Sentjens, cardioloog - intensivist, Flevo Ziekenhuis, Almere, namens de Nederlandse Vereniging voor Cardiologie
- Dhr. dr. F. Jansman, ziekenhuisapotheker - klinisch farmacoloog, Deventer Ziekenhuis, Deventer, en Universiteit Groningen, namens de Nederlandse Vereniging van Ziekenhuis Apothekers
- Dhr. dr. G.E. Jacobs, psychiater - klinisch farmacoloog, Vrije Universiteit Medisch Centrum, Amsterdam en Centre for Human Drug Research, Leiden, namens de Nederlandse Vereniging voor Psychiatrie
- Mw. dr. I.R.A.M. Mertens zur Borg, anesthesioloog, MMT arts, defensie arts, Erasmus Medisch Centrum Rotterdam, namens de Nederlandse Vereniging voor Anesthesiologie, sinds december 2016
Met medewerking van
- Lieve Knarren
- Marjolein Kremers
- Peter Wierenga
- Marjon Verschueren
- Paul Brussee
- Ylonne Sensen
Meelezers
- Prof. dr. D.J. Touw
- Mw. drs. M.E.C. Leenders
Belangenverklaringen
|
Naam |
Hoofdfunctie |
Nevenwerkzaamheden |
Persoonlijke financiële belangen |
Persoonlijke relaties |
Reputatiemanagement |
Extern gefinancierd onderzoek |
Kennisvalorisatie |
Overige belangen |
|
Douwe Dekker |
Internist acute geneeskunde - klinisch farmacoloog |
geen |
geen |
geen |
Aanspreekpunt voor toxicologische onderwerpen binnen Dutch Acute Medicine (DAM, beroepsvereniging voor acute interne geneeskunde) |
Diabetes Fonds; 2007-2010, AGIKO salaris |
Registratie patent voor gebruik van atazanavir als bilirubineverhogend geneesmiddel met anti-inflammatoire, anti-oxidante effecten, publicatie 31-03-2011 |
geen |
|
Dylan de Lange |
Internist-intensivist, UMC Utrecht |
Nationaal Vergiftigingen Informatie Centrum, UMC Utrecht |
Geen conflicterende belangen |
Geen conflicterende belangen |
Geen (conflicterende) belangen |
Geen (conflicterende) belangen |
Geen (conflicterende) belangen |
Geen (conflicterende) belangen |
|
Frank Jansman |
Ziekenhuisapotheker |
Docent en onderzoeker Afdeling Farmacotherapie, Epidemiologi en Economie, Universiteit Groningen; lid METC Isala Zwolle; lid METC Stichting Bebo Assen |
n.v.t. |
n.v.t. |
n.v.t. |
n.v.t. |
n.v.t. |
n.v.t. |
|
Gabriel Jacobs |
Psychiater - klinisch farmacoloog, VU Medisch Centrum, 0,6 FTE |
Klinisch onderzoeker, Centre for Human Drug Research, 0,4 FTE |
geen |
geen |
geen |
Gesponsord geneesmiddelenonderzoek, 2013 - heden, Stichting Centre for Human Drug Research, salaris |
geen |
geen |
|
Henk van Leeuwen |
Internist-intensivist |
|
|
|
|
|
|
|
|
Ingrid Mertens zur Borg |
Anesthesioloog, MMT-arts, defensie anesthesioloog |
Forensisch arts in opleiding |
n.v.t. |
n.v.t. |
n.v.t. |
n.v.t. |
n.v.t. |
n.v.t. |
|
Jan Benedictus |
Beleidsmedewerker Patiëntenfederatie NPCF |
geen |
geen |
n.v.t. |
geen |
geen |
n.v.t. |
geen |
|
Kees Kramers |
Internist-klinisch farmacoloog |
geen |
geen |
geen |
geen |
geen |
geen |
geen |
|
Mariska Tuut |
Eigenaar PROVA (advies-bureau evidence-based richtlijnontwikkeling) |
geen |
geen |
geen |
geen |
geen |
geen |
geen |
|
Roel Sentjens |
|
|
- |
- |
- |
- |
- |
- |
|
Sieuwert Jan ten Napel |
SEH-arts KNMG |
Opleider Spoedeisende Geneeskunde Rijnstate Ziekenhuis Arnhem |
geen |
geen |
geen |
geen |
geen |
geen |
|
Trudy van Dijken |
SEH-arts KNMG St Antonius Ziekenhuis |
|
geen |
geen |
geen |
geen |
geen |
geen |
Inbreng patiëntenperspectief
De inbreng van het patiëntenperspectief werd gewaarborgd door de afvaardiging van een beleidsadviseur van Patiëntenfederatie Nederland in de richtlijnwerkgroep (zie ook de module 'Patiëntenperspectief en nazorg bij intoxicaties').
Methode ontwikkeling
Evidence based
Implementatie
Gedurende het hele proces van richtlijnontwikkeling is rekening gehouden met implementatie van de richtlijn in de praktijk, bijvoorbeeld bij de samenstelling van de werkgroep, de brede knelpunteninventarisatie en de uitgebreide commentaarronde.
Na autorisatie van de richtlijn wordt deze ten minste op de website van de Nederlandse Internisten Vereniging gepubliceerd. Ook andere deelnemende partijen zijn vrij de richtlijn op hun website te publiceren. De richtlijn wordt ter publicatie aangeboden aan www.richtlijnendatabase.nl. Daarnaast wordt getracht samenvattingen van de richtlijn in Nederlandse tijdschriften te publiceren, om zo de implementatie van de richtlijn te bevorderen. De informatie uit deze richtlijn vormt de input voor de herziening van het Acute Boekje van de Nederlandse Internisten Vereniging.
Werkwijze
Knelpuntenanalyse
De richtlijnwerkgroep heeft in de eerste werkgroepvergadering knelpunten in de opvang van patiënten met een acute intoxicatie geïnventariseerd. Daarbij is uitgegaan van het ABCDE-systeem als ‘kapstok’, aangevuld met overige knelpunten. Deze knelpuntenlijst is ter commentaar en aanvulling in een schriftelijke ronde voorgelegd aan de volgende stakeholders:
- Nationaal Vergiftigingen Informatie Centrum
- Nederlandse Internisten Vereniging
- Nederlandse Vereniging voor Ziekenhuisapothekers
- Nederlandse Vereniging voor Psychiatrie
- Nederlandse Vereniging voor Cardiologie
- Nederlandse Vereniging voor Spoedeisende Hulp Artsen
- Nederlandse Vereniging voor Intensive Care
- Nederlands Huisartsen Genootschap
- Patiëntenfederatie Nederland
- Koninklijke Nederlandse Maatschappij ter Bevordering der Pharmacie
- Nederlandse Vereniging van Medisch managers Ambulancezorg / Ambulancezorg Nederland
- Verpleegkundigen & Verzorgenden Nederland
- Event Medical Service
- Nederlandse Vereniging van Ziekenhuizen
- Nederlandse Federatie van Universitair Medische Centra
- Zorgverzekeraars Nederland
- Nefarma
- Inspectie voor de Gezondheidszorg
- Zorginstituut Nederland
- Nederlandse Zorgautoriteit
- Toxicologie.org
De richtlijnwerkgroep heeft de input vanuit de knelpunteninventarisatie geanalyseerd en in de tweede werkgroepvergadering de knelpunten en uitgangsvragen vastgesteld.
Methode richtlijnontwikkeling
De knelpunten en uitgangsvragen zijn uitgewerkt door de verschillende werkgroepleden. Uit explorerend literatuuronderzoek bleek, en dit werd bevestigd door de inhoudelijke experts uit de richtlijnwerkgroep, dat er voor veel knelpunten geen goede evidence voorhanden zou zijn. Het uitvoeren van bewijzend klinisch onderzoek voor deze knelpunten zou in veel gevallen ook een onhaalbare kaart zijn, gezien de vele verstorende en onbekende variabelen die bij acute intoxicaties een rol kunnen spelen.
Derhalve heeft de werkgroep een beperkt aantal vragen aangewezen waarvoor uitgebreid en systematisch literatuuronderzoek heeft plaatsgevonden (verlaagde EMV-score en intubatie, naloxon of intubatie bij opiatenintoxicatie, gebruik flumazenil, behandeling hyperthermie). Bij de uitwerking van deze uitgangsvragen door de richtlijnmethodoloog is uitdrukkelijk aangegeven op welke wijze naar literatuur is gezocht en hoe dit is beoordeeld. Ook na het uitgebreide literatuuronderzoek bleek de beschikbare evidence mager en moest veelal op mechanistische argumenten en klinische redeneringen worden teruggevallen voor het formuleren van aanbevelingen in deze paragrafen. Vanwege de forse kans op vertekening van de resultaten van het literatuuronderzoek, zijn zowel de conclusies als de aanbevelingen niet gegradeerd. De werkgroep constateert dat de evidence over het algemeen van zeer lage kwaliteit is, wanneer gekeken wordt volgens de GRADE criteria (bijvoorbeeld vanwege risk of bias en indirecte studiepopulaties).
Ook bij knelpunten waarvan op voorhand werd verwacht dat er geen evidence zou zijn, en waarbij geen systematisch literatuuronderzoek is uitgevoerd, bleek behoefte aan richtinggevende aanbevelingen. Hierbij is gebruik gemaakt van diverse bronnen (bijvoorbeeld aanpalende evidence) en de mening van experts. Deze knelpunten zijn telkens voorbereid door één of enkele werkgroepleden, waarna door middel van discussie in de richtlijnwerkgroep consensus werd bereikt over het te voeren beleid. Enkele knelpunten zijn door experts van buiten de richtlijnwerkgroep voorbereid. Deze experts zijn genoemd bij de samenstelling van de werkgroep.
De richtlijnwerkgroep is 7 maal bijeen geweest, waarbij conceptteksten werden bediscussieerd en de conceptrichtlijn werd vastgesteld.
Procedure voor commentaar en autorisatie
De conceptrichtlijn is ter commentaar aangeboden aan alle NIV-leden en de (deelspecialistische) verenigingen die bij de ontwikkeling van de richtlijn betrokken zijn. Daarnaast is de conceptrichtlijn ter commentaar verstuurd aan alle partijen die bij de knelpunteninventarisatie om input gevraagd zijn, evenals aan de KNMG-afdeling juridische zaken. Het binnengekomen commentaar is door de werkgroep beoordeeld en verwerkt in de richtlijn. Tijdens de commentaarronde is de werkgroep uitgebreid met een gemandateerde vertegenwoordiger van de Nederlandse Vereniging voor Anesthesiologie.
Daarna is de richtlijn ter autorisatie voorgelegd aan de partijen die in de werkgroep vertegenwoordigd zijn. De richtlijn is geautoriseerd door de Nederlandse Internisten Vereniging, de Nederlandse Vereniging van Spoedeisende Hulp Artsen, de Nederlandse Vereniging van Ziekenhuisapothekers, de Nederlandse Vereniging voor Cardiologie, de Nederlandse Vereniging voor Intensive Care, de Nederlandse Vereniging voor Psychiatrie en de Nederlandse Vereniging voor Anesthesiologie, en heeft tevens de goedkeuring van de Patiëntenfederatie Nederland.
Juridische betekenis van richtlijnen
Richtlijnen zijn geen wettelijke voorschriften, maar op evidence en consensus gebaseerde inzichten en aanbevelingen waaraan zorgverleners moeten voldoen om kwalitatief goede zorg te verlenen. Na autorisatie van de richtlijn door een beroepsvereniging, wordt de richtlijn gezien als deel van de ‘professionele standaard'. Aangezien de aanbevelingen hoofdzakelijk gebaseerd zijn op de ‘gemiddelde patiënt', kunnen zorgverleners op basis van hun professionele autonomie waar nodig afwijken van de richtlijn. Afwijken van richtlijnen kan in bepaalde situaties zelfs noodzakelijk zijn. Wanneer van de richtlijn wordt afgeweken, dient dit beargumenteerd en gedocumenteerd te worden.
Referenties
- Duineveld C, Vroegop M, Schouren L, Hoedemakers A, Schouten J, Moret-Hartman M, et al. Acute intoxications: differences in management between six Dutch hospitals. Clin Toxicol 2012; 50: 120-8.
- Lanting LC, Stam C, den Hertog PC. Hoe vaak komt zelf toegebracht letsel voor en hoeveel mensen sterven eraan? In: Volksgezondheid toekomst verkenning. Nationaal Kompas Volksgezondheid. http://www.nationaalkompas.nl/gezondheid-en-ziekte/ziekten-en-aandoeningen/letsels-en-vergiftigingen/zelftoegebracht-letsel/omvang/
Zoekverantwoording
Zoekacties zijn opvraagbaar. Neem hiervoor contact op met de Richtlijnendatabase.
